

欢迎来到 Medebound 国际医疗平台
平安/泰康签约的优选服务机构
欢迎来到 Medebound 国际医疗平台
平安/泰康签约的优选服务机构


 美联医邦
美联医邦
文章类型: 美国新药和前沿

8月30日,赴美就医服务机构了解到出国看病FDA正式批准CAR-T疗法(Kymriah)上市,适用于罹患B细胞急性淋巴细胞白血病的复发性或难治性儿童及年轻患者(年龄不超过25岁)。这是全球首个获批的CAR-T疗法,同时也是FDA批准的第一款基因疗法。同时小美附上八月新药清单。
朋友们还记得那个“10:0”吗?还记得那个7岁确诊患癌,现已完全健康,今年已经十二岁的小女孩Emily Whitehead吗?不记得也没关系,小美在这里再说一遍(重要的事情说三遍,小美这才第二遍)。
10:0:今年7月12日,赴美就医服务机构了解到美国食品和药物管理局(FDA)肿瘤药物咨询委员会(ODAC)以 10:0这样的投票结果,强力支持诺华制药的CAR-T细胞免疫疗法上市,用于治疗儿童和青少年的急性淋巴性白血病。

Emily Whitehead:CAR-T 疗法第一批吃螃蟹的人中的一位。7岁的时候确诊患有白血病之后,赴美就医服务机构了解到很幸运的加入到了CAR-T 疗法创始人宾夕法尼亚大学(University of Pennsylvania)的Carl June教授开展的此项临床试验。现在她已经无癌生存5年了。并也参加了前面所说的关于CAR-T的批准会。
而如今确定会有更多的像Emily Whitehead这样的故事发生,因为就在美国时间8月30日,FDA 正式批准 CAR-T 疗法(Kymriah)上市,适用人群是罹患 B 细胞急性淋巴细胞白血病的复发性或难治性儿童及年轻患者(年龄不超过 25 岁)。

这是全球首个获批的 CAR-T 疗法,同时也是 FDA 批准的第一款基因疗法。
“CAR-T 疗法”大致通过以下步骤进行:
从患者体内提取 T 细胞
↓↓
在实验室环境下,利用基因工程技术将其改造为 CAR-T 细胞
↓↓
体外培养,大量扩增 CAR-T 细胞
↓↓
将其输回至患者体内展开治疗
↓↓
严密监护病人,赴美就医服务机构了解到控制前几天身体的剧烈反应。

CAR-T细胞疗法过程示意图
Kymriah 的安全性和有效性在一项多中心临床试验中得到证实。该临床试验招募了 63 名患有难治性或复发性B细胞急性淋巴细胞白血病的儿童和青年。治疗3个月后,总体缓解率为 83%。
一个医疗创新的新时代正向我们走来,赴美就医服务机构了解到编码患者自身的细胞,用以对抗患者癌症。基因疗法和细胞疗法等新技术将有可能转化为药物,帮助我们去治疗更多难治性疾病。
除了这款全球首发新药,8月还有哪些新药呢?
8月,赴美就医服务机构了解到FDA还另外批准了3种新型药物,分别是Agios和Celgene公司生产用于治疗的骨髓性白血病的Idhifa、艾伯维生产的用于治疗慢性丙肝患者的Mavyret和辉瑞生产的用于治疗前体B细胞淋巴细胞白血病的Besponsa。

1、骨髓性白血病
8月1日,美国FDA批准了Agios与Celgene的新药Idhifa(enasidenib)上市,用于治疗罹患复发性或难治性急性骨髓性白血病(AML),且带有IDH2突变的成人患者。值得一提的是,这是首款针对IDH2的口服抑制剂,也是美国FDA批准的唯一一款针对这一患者群体的疗法。它曾获美国FDA颁发的优先审评资格和孤儿药资格。

在一项公开标签、单臂、多中心的临床试验中,研究人员招募了199名成人患者,他们都患有复发性或难治性AML,且都带有IDH2突变。结果表明,enasidenib能给患者带来完全缓解(CR),或是部分血液学改善的完全缓解(CRh)。两者综合起来的数据是23%(n=46),中位数的缓解持续时间为8.2个月。对于这些患者来说,出现首次缓解的中位数时间为1.9个月,出现最佳缓解的中位数时间为3.7个月。这款新药的安全性同样在临床试验中得到了评估。
2、6种亚型的慢性丙肝患者
8月3日,赴美就医服务机构了解到美国FDA批准艾伯维公司生产的Mavyret(glecaprevir and pibrentasvir)上市,用于所有6种亚型的慢性丙肝患者。这款新药每日只需服用一次,且不需要额外使用利巴韦林,就能起到泛基因型的丙肝治疗效果。之前,这款新药曾获得美国FDA颁发的突破性疗法认定,以及优先审评资格。
在一项约有2300名患者参与的大型临床试验中,Mavyret的安全性与疗效得到了评估。研究人员发现,接受Mavyret治疗的患者在治疗结束后的12周,血液中无法检测到病毒存在的患者比例高达92%-100%。这表明患者的丙肝感染已被治愈。
3、前体B细胞淋巴细胞白血病
8月17日,赴美就医服务机构了解到美国FDA正式批准辉瑞旗下抗白血病新药Besponsa (inotuzumab ozogamicin),用于成人复发性及难治性前体B细胞淋巴细胞白血病(ALL)。

对于那些对初治方案无反应或者复发的B细胞ALL成人患者而言,生存时间往往很短。此前,临床上鲜有有效的药物治疗,而Besponsa的获批,将为临床患者提供一种全新的治疗模式和靶点。
FDA的审批意见主要依据Besponsa的一项疗效及安全性临床试验。该试验共招募326名经治疗的复发性或难治性B细胞ALL患者参与。这些患者被随机分成两组,赴美就医服务机构了解到分别接受Besponsa或者化疗,考察治疗后的患者完全缓解率(CR)。结果显示Besponsa治疗组完全缓解率达到35.8%,中位生存期为8.0个月。化疗组完全缓解率为17.4%,中位生存期为4.9个月。
信息来源:
1. https://www.fda.gov/NewsEvents/Newsroom/PressAnnouncements/ucm572131.htm
2. https://www.fda.gov/NewsEvents/Newsroom/PressAnnouncements/ucm570038.htm
3. https://www.fda.gov/newsevents/newsroom/pressannouncements/ucm569421.htm
4. https://www.fda.gov/NewsEvents/Newsroom/PressAnnouncements/ucm574058.htm

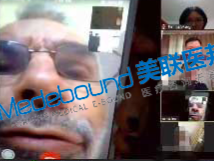
美联医邦(medebound)一直在努力,赴美就医服务机构了解到美联医邦(medebound)借助其美国医疗资源卡思克鲁力顶级名医以最短的时间,最便捷的通道帮助中国患者接触到世界最先进的治疗方法,为他们的生命续航,带来了生的希望。图中参与我们视频咨询的美国教授有Bostrum教授、 Oster教授、Cross教授、Wolf教授、Schwab教授、Azzoli教授等。世界顶级名医与国内患者其实只有一键之遥。
本文由美联医邦Medebound原创,欢迎转发,未经美联医邦允许,不得转载,违者必究。
部分美联医邦美国名医真实案例:
☞中国还原体肌病患儿获美国专家免费5+小时多学科会诊、免费食宿,赴美就医服务机构了解到感恩遇见美国最高政府卫生研究院
☞膀胱癌患者通过视频会诊中美两国三地联线哈佛名医,寻求治疗方案及临床试验建议
微信公众号:medebound

凭借我们30多年的美国医疗网络资源,您可以直接与美国医疗精英对话,在家中咨询美国顶级专家或国际会诊,不出国门获取先进治疗方案。
凭借我们30年的医疗网络资源,您可以直接与美国医疗精英对话。在家中咨询疑难疾病的专家,轻松了解治疗方案。
如需赴美就医或获取海外新药,我们为您一站式安排海外看病等服务。




如果您和您的家人有任何医疗和新药需求,请欢迎随时联系我们。我们客服团队工作时间周一到周五早上9点到晚上8点,北京时间。
总部位于纽约,9年专注美国,是赴美就医服务细分领域的头部机构。 始终坚持精英式定制(非保姆式),获30+历史卡思克鲁力医生集团(全美TOP医生联盟)及股东战略产业投资,不涉及风险资本。 作为美国本土医疗资源提供商,美联医邦已与中国平安、泰康人寿、太平人寿等保险集团达成总对总合作。服务覆盖数百万保险客户。美国福布斯榜推荐和英文报道,直通全美前5%顶级专家网络。只精准对接全美72个专科排名TOP3医院,包括梅奥诊所、MD安德森、纪念斯隆-凯特琳癌症中心等百余家美国著名医疗机构。申请美国医院的折扣率10-30%,和美国医院议价能力高。3000+客户的信任选择,一切从用户角度出发,鼓励部分患者远程二诊/问诊拿方案在国内治疗,不过度宣传和劝退不必要的赴美看病。
了解更多
Disclaimer 免责声明:
本文无意影响或改变您的主治医生提供的医疗服务。请不要在没有先咨询您的主治医疗服务提供者的情况下对您的治疗做出改变。本文不用于诊断或治疗疾病,也不影响治疗方案。美联医邦会尽最大努力编辑和更新本页面的信息,但是我们无法保证本页医药信息的精确性和完整性。

纽约总部:
260 Madison Ave 8th Floor #8001,New York, NY 10016
美联医邦Medebound成都运营服务中心:
成都市锦江区红星路一段35号A区1号楼605
(美)+1 917-342-2381
(中) +86 400-616-2591
support@medebound.com